Home / 제품소개 / 상세페이지

COVID-19 total Ab 정성검사
- U.S. FDA EUA 승인
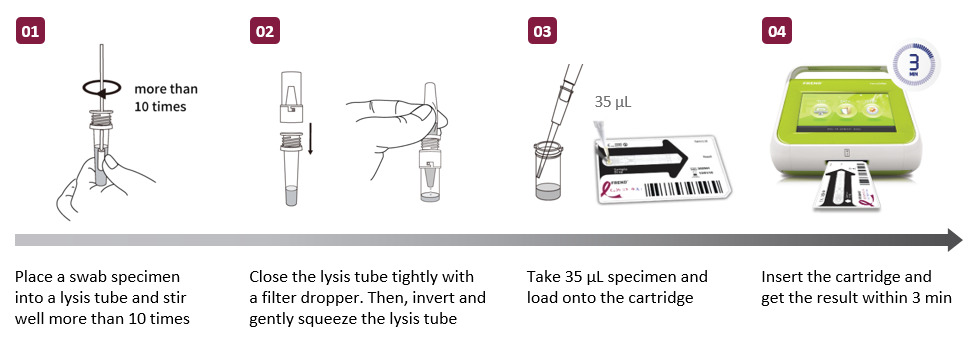
- 3분 내 COVID-19 total Ab 정성 검사
- 총 2단계의 손쉬운 사용
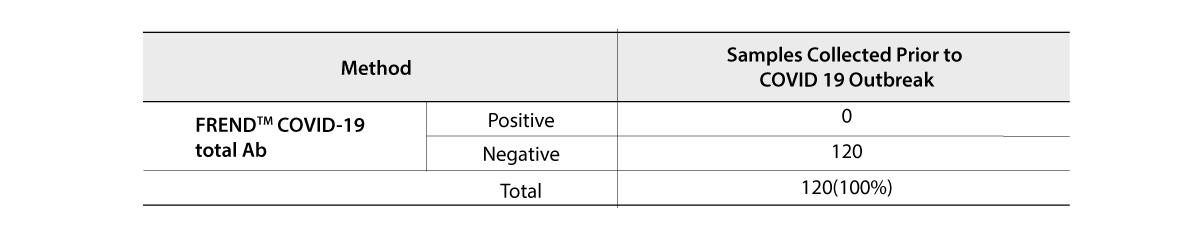
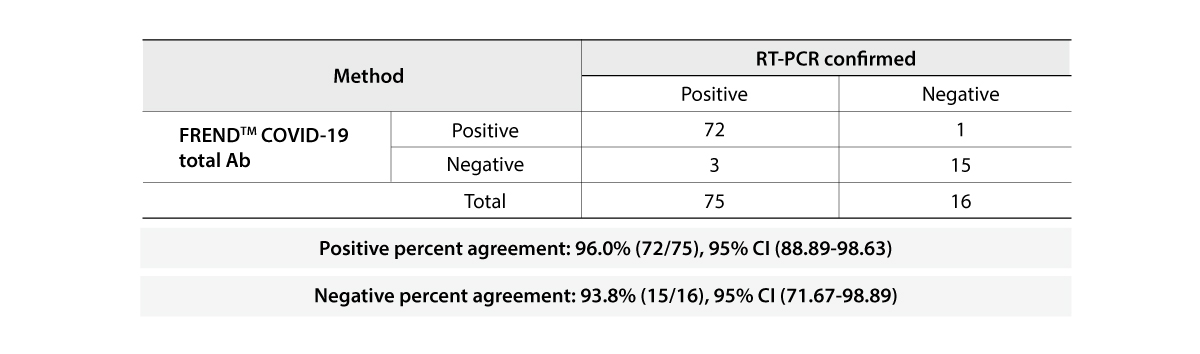
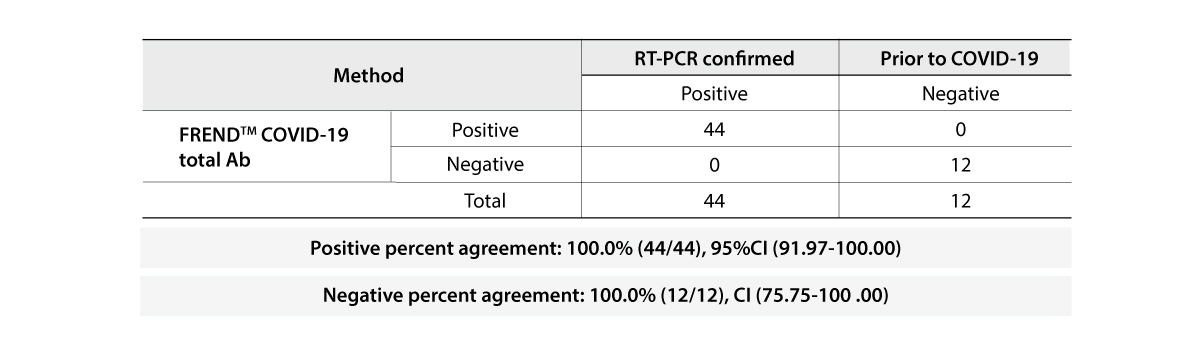
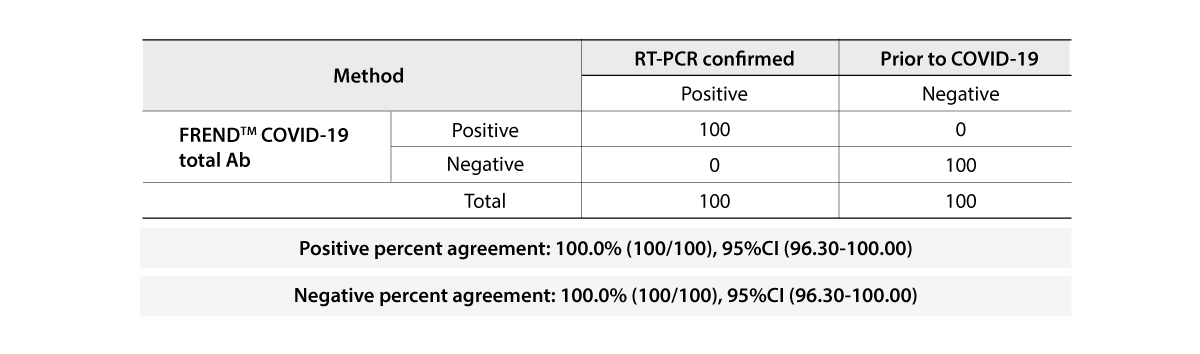
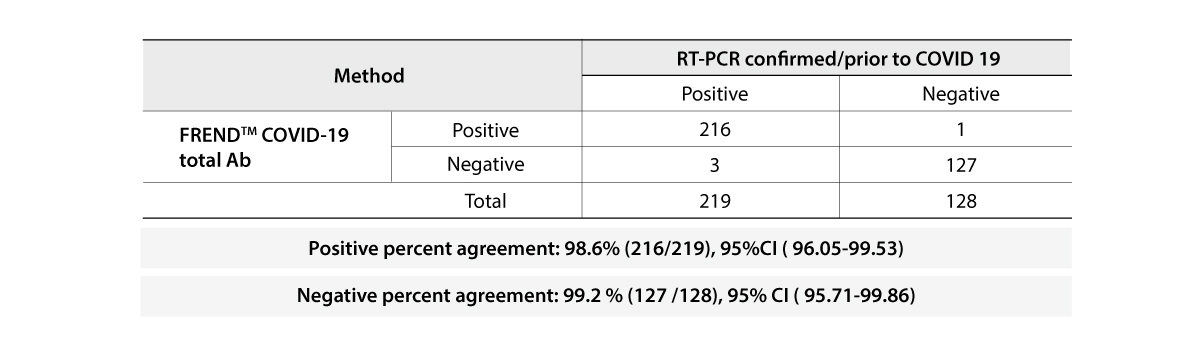
- 양성 정확도 96.7%, 음성 정확도 98.8%
- 형광면역측정법 정성 분석
- LIS connectivity (임상병리정보시스템)
*본 제품은 수출용 허가를 받은 제품입니다.
The FREND™ COVID-19 total Ab는 사람의 혈청 및 혈장(EDTA, Heparin, Citrate)에서 신종 코로나 바이러스(COVID-19)의 IgG와 IgM항체를 형광면역측정법으로 정성 분석하여 신종 코로나 바이러스 감염 확인에 도움을 주는 체외진단 의료기기입니다.

3분 이내로 쉽고 빠르게 검사 결과를 제공하여 신속한 의사결정을 돕습니다.
Effective Data Management
• Not for the screening of donated blood.
Visit NanoEntek blog now!
Want to learn more about cell counting and cell therapy?
Visit to find out more!
-
Assay method
Fluorescent immunoassay
-
Cat. No.
FRCOA 020
-
Specimen
EDTA Plasma
-
Volume
35 μL
-
Time to result
Cartridge reaction : < 3 min
-
Package
20 tests
-
Storage condition
2–8 °C (35–46 °F)

ExTransfection™ Protocol Library
ExTransfection™은 사용자가 손쉽게 실험을 설정하고 수행할 수 있도록 오픈 프로토콜을 제공합니다. 24-well 최적화 방식을 통해 transfection 프로토콜을 빠르고 간단하게 최적화할 수 있습니다.
또한 adherent과 suspended cells 모두에 대해 전기적 매개변수를 효율적이고 신속하게 최적화할 수 있는 사전 프로그래밍 된 최적화 프로토콜이 포함되어 있습니다.

 KOR
KOR ENG
ENG































